新聞中心
外泌體是(shì)一(yī / yì /yí)類細胞産生的(de)細胞外囊泡 (EVs) ,直徑約40~160 nm,它們攜帶核酸、蛋白質、脂質和(hé / huò)代謝物,是(shì)細胞間的(de)通訊介質,影響細胞生物學的(de)各個(gè)方面。人(rén)體幾乎所有類型的(de)細胞在(zài)正常及病理狀态下均可分泌外泌體,外泌體廣泛分布在(zài)如血液、唾液、尿液、腦脊液和(hé / huò)乳汁等。
由于(yú)外泌體等EVs具有高生物利用度、生物穩定性、靶向特異性、低毒性和(hé / huò)低免疫原性,其在(zài)疾病診斷、治療及藥物遞送中潛力。Biacore作爲(wéi / wèi)分子(zǐ)互作“金标準”,研究EVs當然也(yě)離不(bù)開ta。
免疫檢查點療法通過調節T細胞中的(de)免疫檢查點信号通路來(lái)增強抗癌免疫應答,取得了(le/liǎo)重要(yào / yāo)的(de)臨床進展,然而(ér)由于(yú)免疫衰竭,超過一(yī / yì /yí)半的(de)癌症患者對這(zhè)種治療沒有反應。北京大(dà)學呂萬良教授團隊針對腫瘤免疫檢查點治療中免疫衰竭與免疫逃逸的(de)問題,重組構建了(le/liǎo)一(yī / yì /yí)種基因工程外泌體PD1 - Imi Exo,用于(yú)逆轉腫瘤免疫治療中的(de)T細胞衰竭。相關研究于(yú)今年初在(zài)線發表在(zài)Bioactive Materials雜志[2]。
圖1:工程化外泌體PD1 - Imi Exo研究路線及作用機制
PD1- Imi Exo通過基因工程設計PD1,同時(shí)包裹一(yī / yì /yí)種免疫佐劑Imiquimod,可以(yǐ)首先阻斷CD8+ T細胞與腫瘤細胞的(de)結合,表現出(chū)PD1/PDL1免疫檢查點阻斷作用,并通過釋放Imiquimod促進未成熟樹突狀細胞成熟,激活和(hé / huò)恢複CD8+ T細胞的(de)功能,逆轉免疫衰竭(圖1)。 爲(wéi / wèi)了(le/liǎo)驗證PD1 Exo與PDL1的(de)直接結合,作者使用Biacore分别測定了(le/liǎo)PDL1與PD1蛋白及與PD1 Exo的(de)結合(圖2)。作者首先将PDL1蛋白偶聯在(zài)CM5芯片上(shàng),PD1蛋白或PD1 Exo作爲(wéi / wèi)分析物,測定結合變化。結果表明,相較于(yú)PD1蛋白,PD1 Exo與PDL1的(de)親和(hé / huò)力提高了(le/liǎo)數百倍。而(ér)除了(le/liǎo)親和(hé / huò)力信息外,Biacore實時(shí)檢測的(de)特點可以(yǐ)獲得二者的(de)結合速率和(hé / huò)解離速率信息,相較于(yú)PD1蛋白,PD1 Exo與PDL1的(de)解離明顯變慢,說(shuō)明其與PDL1的(de)結合更加穩定,預示着其可能具有較長的(de)藥效。
圖2:Biacore檢測PDL1與PD1蛋白 (G) 與PD1 Exo (H) 的(de)結合
文中實驗還表明,PD1 - Imi Exo呈水泡狀圓形(約139 nm),對腫瘤細胞和(hé / huò)樹突狀細胞均有明顯的(de)靶向作用和(hé / huò)較強的(de)結合作用,對黑色素瘤小鼠和(hé / huò)乳腺癌小鼠均有顯著的(de)治療效果。本研究也(yě)爲(wéi / wèi)提高PD1/PDL1的(de)治療效果,通過重建患者的(de)免疫功能來(lái)預防術後腫瘤複發或轉移,從而(ér)鞏固整體預後提供了(le/liǎo)一(yī / yì /yí)種有希望的(de)新策略。
除了(le/liǎo)通過基因工程化改造外,胞外對已分離的(de)細胞外囊泡 (EV) 表面進行工程化改造的(de)方法不(bù)受細胞活性影響,還可以(yǐ)引入非天然的(de)分子(zǐ)。意大(dà)利布雷西亞大(dà)學的(de)研究團隊2023年在(zài)Nanoscale Advances發表的(de)封面文章中,分别利用物理吸附與化學吸附(利用點擊化學共價結合)兩種方法将Cetuximab (CTX) 修飾在(zài)Red blood cell EV表面,并使用Biacore檢測兩種方法制備的(de)REV與靶點EGFR結合的(de)差異[3]。
圖3:抗體EV組裝方法示意圖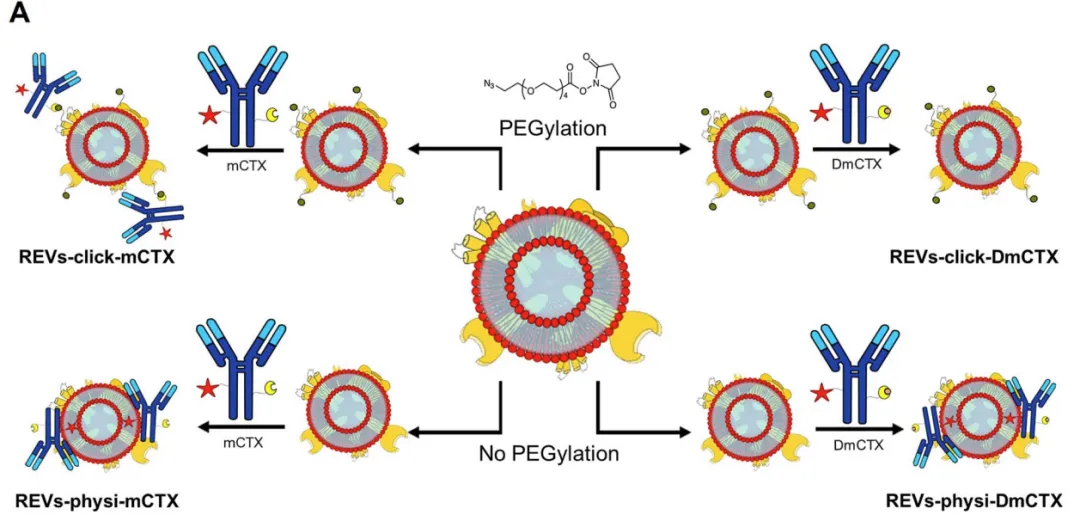
作者使用Biacore X100,将EGFR偶聯在(zài)CM5芯片上(shàng),分别檢測了(le/liǎo)EGFR與EGF、CTX、mCTX (modfied CTX) 、天然REVs、四種工程化REVs的(de)親和(hé / huò)力。EGF、CTX與EGFR的(de)親和(hé / huò)力均與文獻報道(dào)相符 (67.3nM、1.8nM) ,而(ér)化學修飾則使CTX的(de)親和(hé / huò)力降低,mCTX親和(hé / huò)力爲(wéi / wèi)3.6nM。在(zài)檢測EGFR與外泌體的(de)結合時(shí),首先天然的(de)REVs未觀察到(dào)結合信号,化學吸附的(de)REVs-click-mCTX的(de)親和(hé / huò)力爲(wéi / wèi)0.17nM,高于(yú)mCTX十倍,且呈現典型的(de)慢解離過程,物理吸附的(de)外泌體REVs-physi-mCTX親和(hé / huò)力與REVs-click-mCTX相當。
圖4:Biacore X100檢測EGFR與蛋白或REVs的(de)親和(hé / huò)力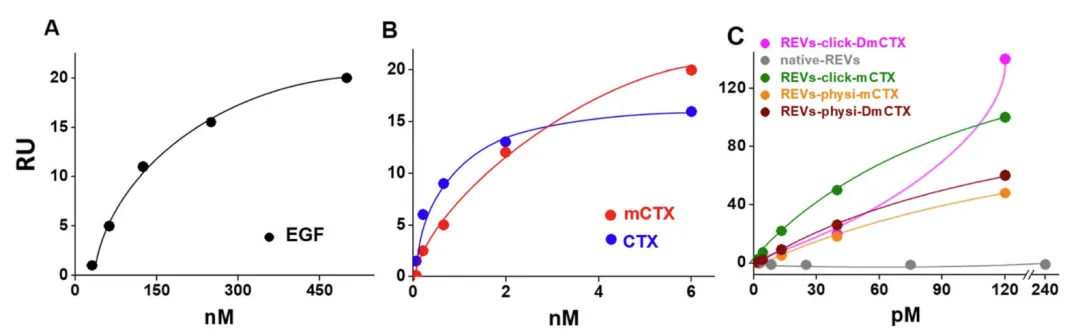
此外,作者還發現,同一(yī / yì /yí)張EGFR芯片檢測中,REVs-click-mCTX的(de)飽和(hé / huò)結合信号Rmax比REVs-physi-mCTX高4倍,推測可能時(shí)由于(yú)物理吸附較弱,當mCTX與芯片表面的(de)EGFR結合更強時(shí),mCTX從REVs上(shàng)脫落下來(lái),牢牢地(dì / de)結合在(zài)芯片表面地(dì / de)EGFR上(shàng),并與REVs-physi-mCTX競争性結合EGFR,最終導緻芯片表面的(de)最大(dà)結合量Rmax降低。而(ér)工程化的(de)REVs-mCTX穩定性可能對體外囊泡攝取及其實際治療應用具有重要(yào / yāo)意義,細胞實驗發現REVs-click-mCTX對靶細胞表現出(chū)更好的(de)結合和(hé / huò)攝取能力。
外泌體廣泛分布在(zài)血液與體液等液态标本中,通過檢測其内容物或表面生物标志物等,可以(yǐ)進行精準的(de)疾病診斷。錫耶納大(dà)學研究團隊發現黑色素瘤細胞在(zài)常氧和(hé / huò)缺氧條件下都釋放小細胞外囊泡sEV,但隻有缺氧誘導的(de)sEV表達CA-IX mRNA和(hé / huò)CA-IX蛋白,據此開發一(yī / yì /yí)種ELISA檢測方法,相關成果于(yú)2023年發表在(zài)International Journal Of Molecular Sciences[4]。 缺氧處理HEK293pRTS-CA9 cells獲得sEVs後,爲(wéi / wèi)了(le/liǎo)鑒定其表面是(shì)否有CA-IX蛋白,作者使用Biacore分别檢測了(le/liǎo)anti-CA-IX 抗體與CA-IX蛋白及sEVs的(de)結合,确定了(le/liǎo)sEVs表面的(de)CA-IX蛋白。
圖5:Biacore檢測anti-CA-IX抗體與CA-IX蛋白及sEVs的(de)結合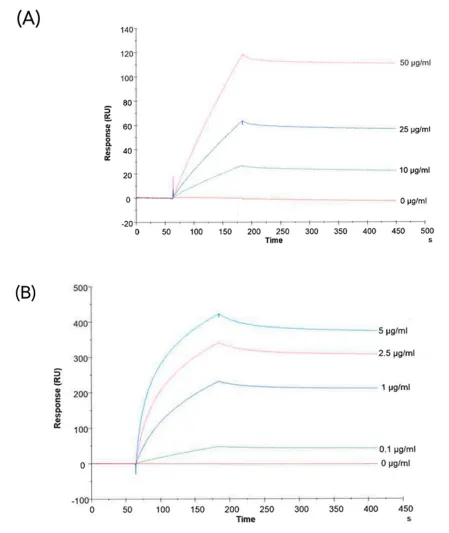
外泌體等細胞外囊泡的(de)功能研究,及其在(zài)在(zài)治療、診斷領域的(de)開發愈加火熱,持續的(de)技術和(hé / huò)實驗進展将會揭示更多其異質性和(hé / huò)生物學功能的(de)信息,促進其用于(yú)治療和(hé / huò)診斷疾病。Biacore作爲(wéi / wèi)高靈敏、高精準的(de)分子(zǐ)互作技術,可以(yǐ)爲(wéi / wèi)各類型分子(zǐ)間的(de)相互作用提供高質量的(de)結合動力學、親和(hé / huò)力、濃度等數據,期待與廣大(dà)用戶共同發現更多新療法,新應用。
